隨著醫療器械的智能化發展,軟件的應用和研究也越發廣泛,國家的監管也越來越嚴格,在上市前研發注冊及后期的質量控制環節中都有其特殊要求。近年來,國家也相繼出了醫療器械軟件產品相關的法規、標準和指南性文件。
為了在工作中更好的進行醫用軟件的開發、測試及管理、幫助醫療器械生產企業規范應對醫療器械軟件技術驗證、網絡安全的風險控制、生產質量管理體系建立及注冊申報。瑞旭集團-北京西爾思科技有限公司特聯合中檢集團南方測試股份有限公司于2023年3月30日舉辦一期醫療器械產品醫用軟件國內注冊研討會。
會議議題
-醫療器械軟件法規規范概述
-醫療器械軟件網絡安全技術,滲透,漏洞解析
-數字療法產品注冊解析
-醫療器械軟件臨床評價要點解析
-遠程醫療發展趨勢
-案例分享與現場答疑
會議安排
會議時間:2023年3月30日14:00-17:00
會議方式:線下會議
會議地址:深圳市南山區西麗街道沙河路43號電子檢測大廈B棟5樓培訓室
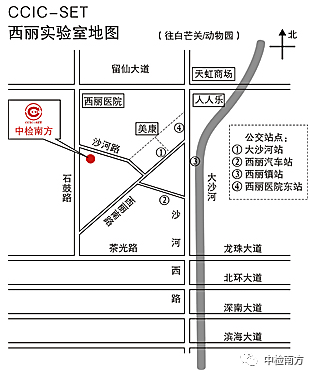
5號線環中線西麗站A出口或者7號線茶光站B出口。步行10分鐘可到中檢南方。
培訓收費:免費
參會名額:100人 (請大家火速報名,報滿即止)
報名方式:請聯系下方人員參會報名。
姓名:王艷
電話:0755-86097059
電郵:sophie.wang@ccic-set.com
(報名人員請3月29日之前發送報名信息:公司名稱、姓名、職務、聯系電話、手機、郵箱至我司活動聯系人郵箱。)
參會企業可通過添加以下微信加入討論群--“軟件注冊群”

講師介紹
傅賽珍
瑞旭集團醫療器械事業部 副總經理
國家認證的醫療器械注冊工程師,醫療器械質量體系審核師;
10年以上醫療器械體系、注冊、臨床評價及合規輔導工作經驗,對有源醫療器械、人工智能及數字療法軟件、可吸收植入材料等產品合規注冊和臨床評價有豐富的經驗,組織完成數百個產品的合規和注冊工作。
陳海鑫
軟件產品質量檢驗師,高級性能測試工程師,9年第三方軟件檢測從業經驗
熟悉了解GB/T 25000.51等軟件國家標準,國家CMA-軟件領域授權簽字人
CNAS-軟件領域授權簽字人,中檢南方軟件評測中心負責人
主辦單位簡介
瑞旭集團
瑞旭集團(CIRS)創立于2007年,是一家專業的產品合規技術咨詢服務機構,其總部位于中國杭州,在愛爾蘭、英國、美國、韓國及中國北京、上海和南京設有分支機構。
醫療器械事業部瑞旭集團旗下專業的醫療器械技術服務平臺,專注于為國內外醫療器械企業提供研發生產、檢測驗證、臨床評價、質量管理體系及注冊申報(認證)等全產業鏈技術服務。瑞旭集團配置醫療器械專業技術服務團隊:醫療器械研發生產技術團隊、檢測評價技術團隊、臨床評價技術團隊、臨床醫學技術團隊、臨床統計與數據管理團隊、臨床運營管理團隊、法規事務(注冊&體系)團隊,為醫療器械企業提供從研發生產到臨床注冊的一站式合規技術服務。
中檢南方
中檢集團南方測試股份有限公司(以下簡稱:中檢南方)于1985年成立,是中國檢驗認證集團(中檢集團、CCIC)的控股企業。經過近30年的努力奮斗,已成功獲得了“國家級質量認證合格單位(CMA)”、“食品檢驗機構資質認定(CMAF) ”、“中國合格評定國家認可委員會(CNAS)認可實驗室”、“國家強制性產品(3C)指定檢測機構”、“國家節能產品認證指定檢測機構”、“高新技術產品成果鑒定指定檢測單位”、“深圳市電子產品質量監督檢驗機構”、“中國質量認證中心(CQC)簽約實驗室”、“國家能源光伏發電設備評定中心”、“國推RoHS指定實驗室”、“CB實驗室”、“大眾、一汽專業第三方測試機構”、“TUV Rheinland授權第三方測試實驗室”、“GCFRTO實驗室”、“NVLAP認可實驗室”等20余項國內外重要資質,并建立了佛山分公司,蘇州、青島、成都3個辦事處。
中檢南方擁有具國際先進水平的10米法、5米法電波暗室各一個、天線性能測試暗室(OTA)一個、3米法電波暗室二個;填補華南地區空白的SAR實驗室一個,高清數字電視實驗室一個、光伏電池(PV)認證測試實驗室一個、藍牙產品認證測試室一個;還有完全符合國際標準的RoHS實驗室、頗具實力的安全實驗室、完善的環境與可靠性試驗室以及與世界先進水準同步的性能測試室等。所配置的儀器設備、測試系統均屬當今世界一流品牌、一流水準。并擁有一支高學歷、高素質、高效率、業務精通、經驗豐富的專業檢測(科研)隊伍和寬松的檢測場地。http://www.ccic-set.com/
